Oxidação
Índice
A oxidação é um processo químico que ocorre quando se perdem electrões de uma molécula, átomo ou ião. No contexto da calorimetria, a oxidação é frequentemente analisada como uma análise térmica, que envolve a queima ou decomposição de substâncias para libertar energia sob a forma de calor.
A Calorimetria Exploratória Diferencial (DSC)
é uma técnica que pode ser utilizada para caraterizar este processo, uma vez que mede o fluxo de calor associado à oxidação de uma amostra durante o aquecimento ou arrefecimento. O princípio subjacente à medição da oxidação com a DSC (Calorimetria Exploratória Diferencial) baseia-se na natureza exotérmica das reacções de oxidação.
Na DSC, a oxidação pode ser estudada de forma isotérmica ou não isotérmica. Para estudos de oxidação isotérmica, a temperatura do cadinho da amostra DSC é definida a uma temperatura constante e a oxidação da amostra é monitorizada ao longo do tempo.
O início da oxidação é normalmente indicado pelo aparecimento de um pico exotérmico na curva DSC, que corresponde à libertação de calor à medida que a amostra oxida. O tempo em que ocorre o pico exotérmico é designado por tempo de indução da oxidação (OIT) e é uma medida da resistência da amostra à oxidação. O método é ilustrado na Fig. 1.
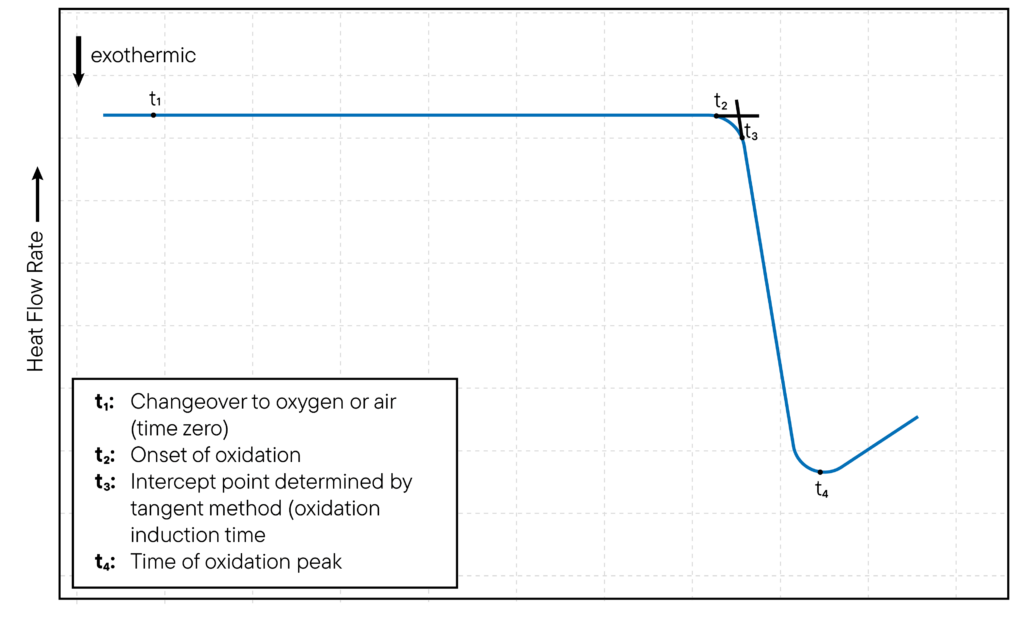
Nos estudos de oxidação não isotérmica, a temperatura da célula DSC é aumentada a uma taxa constante e a oxidação da amostra é monitorizada em função da temperatura.
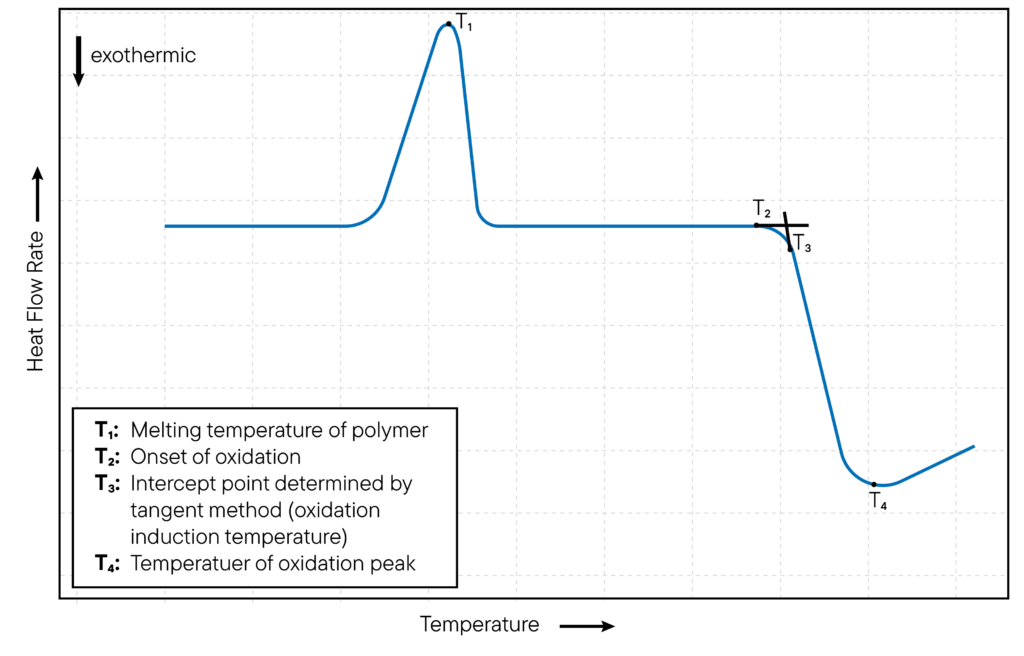
O dispositivo DSC detecta um pico exotérmico na curva DSC quando uma amostra oxida e liberta calor. A temperatura a que o pico ocorre é referida como a temperatura de início da oxidação (OOT).
O método é apresentado na Fig. 2. O OOT é uma medida da estabilidade térmica da amostra e é utilizado para avaliar a estabilidade oxidativa dos materiais.
Resumindo, medindo o tempo de indução da oxidação (OIT) ou a temperatura de início da oxidação (OOT) a diferentes temperaturas, a energia de ativação para a oxidação pode ser determinada, o que fornece informações sobre a estabilidade térmica da amostra.
A DSC também pode ser utilizada para avaliar os efeitos dos antioxidantes e outros aditivos na estabilidade oxidativa das amostras, o que é importante para a sua qualidade e prazo de validade.
A DSC também pode ser utilizada para determinar a energia de ativação para a oxidação, que é uma medida da energia necessária para iniciar o processo de oxidação.
A energia de ativação pode ser calculada utilizando a equação de Arrhenius, que relaciona a velocidade de uma reação química com a temperatura a que esta ocorre. A energia de ativação para a oxidação pode ser determinada medindo o tempo de indução da oxidação (OIT) ou a temperatura de início da oxidação (OOT) a diferentes temperaturas e traçando os dados num diagrama de Arrhenius.
O declive da linha resultante é utilizado para calcular a energia de ativação para a oxidação. A curva DSC pode ser analisada para determinar vários parâmetros relacionados com a oxidação, por exemplo, a temperatura inicial, a temperatura de pico e o calor de oxidação.
Tanto o OIT como o OOT são parâmetros importantes para avaliar a estabilidade à oxidação dos materiais, e a eficácia dos antioxidantes pode ser comparada, especialmente em polímeros.
Um OIT mais longo ou um OOT mais elevado indica uma maior estabilidade oxidativa e resistência à degradação. Os factores que podem afetar a precisão das medições DSC para a oxidação incluem a preparação da amostra, a instrumentação e as condições experimentais, como a taxa de aquecimento e a atmosfera.
A análise térmica pode ser utilizada para estudar a oxidação de metais numa atmosfera que contenha oxigénio, onde se forma um óxido metálico e o aumento de massa dependente da temperatura ou do tempo pode ser observado utilizando técnicas como a TGA.
Decomposição durante a oxidação
Referencias:
- Stephen M. Hsua e Chun-I Chenb, Um modelo de cinética química para prever o desempenho do motor diesel. Parte II. Procedimentos de teste de bancada: Tribology Letters, Vol. 14, No. 2, fevereiro de 2003.
- B. Wunderlich, Thermal Analysis of Polymeric Materials (Análise térmica de materiais poliméricos). Berlim, Heidelberg: Springer-Verlag Berlin Heidelberg, 2005.
- G. W. Ehrenstein, G. Riedel e P. Trawiel, Thermal analysis of plastics: Theory and practice. Munique: Hanser, 2004.
- Plásticos – Calorimetria Exploratória Diferencial (DSC), ISO 11357-6, 2008.
- Mahbuba Islam, Anna Kaczmarek, and Jolanta Tomaszewska-Gras, Differential scanning calorimetry as a tool to assess the oxidation state of cold-pressed oils during shelf-life: Journal of Food Measurement and Characterization (2023) 17:6639-6651.