La formula chimica del gesso è CaSO4 ∙ 2H2O(solfato di calcio diidrato). Gli usi del gesso come materiale da costruzione sono molteplici.
Il gesso è una polvere secca che viene mescolata con acqua per formare una pasta che poi si indurisce. Dopo l’essiccazione rimane abbastanza morbido e può essere facilmente lavorato con strumenti metallici.
Il solfato di calcio emiidrato (CaSO4 ∙ ½H2O) reagisce con l’acqua per formare solfato di calcio diidrato e viceversa Il solfato di calcio diidrato separa l’acqua quando viene riscaldato e la scambia con il solfato di calcio emiidrato.
La scindibilità del CaSO4 ∙ 2H2Ocristallino è dovuta ai bilayer di CaSO4(in ogni strato gli ioni Ca2 + e SO4 2 si trovano alternativamente uno accanto all’altro) con legami idrogeno relativamente bassi.
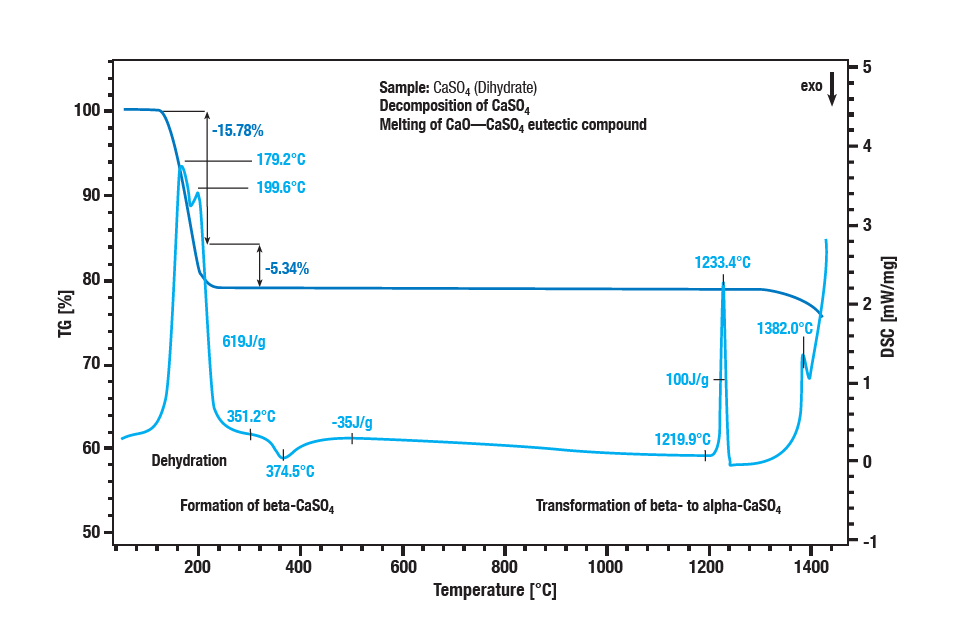
La disidratazione in due fasi del solfato di calcio diidrato avviene tra i 100 °C e i 300 °C. La prima fase è la formazione di emiidrato (CaSO4 ∙ 2H2Oa CaSO4 ∙ ½H2O).
Un’ulteriore disidratazione forma l’anidrato (CaSO4 ½ H2Oa CaSO 4). Con un effetto esotermico a circa 340 °C, l’anidrato si converte in β-solfato di calcio. L’effetto esotermico nella curva a circa 1220 °C è la conversione del β-solfato di calcio in α-solfato di calcio. La decomposizione del solfato si riflette in un’ulteriore perdita di massa a temperature superiori ai 1250 °C.
Il solfato di calcio viene convertito in ossido di calcio. La fusione di una miscela eutettica di solfato di calcio e ossido di calcio raggiunge un picco a 1380 °C.
Dispositivo di misurazione adatto
STA L81 -
TG + DSC
STA ad alta temperatura con configurazione del forno fino a 2400°C

