Entalpi
Entalpi – termal analizde ölçülen bir değişken
Entalpi nedir?
Reaksiyon entalpisi, bir kimyasal reaksiyon sırasında bir numunenin entalpi değişimidir. Enerjinin ısı şeklinde açığa çıktığı reaksiyonlar ekzotermik olarak adlandırılır. Enerjinin sağlanması gereken reaksiyonlar endotermik olarak adlandırılır.
Erime entalpileri endotermik süreçlerin basit bir örneğidir, çünkü katı kristal yapısını parçalamak ve birbirlerine göre serbestçe hareket edebilen moleküllere sahip sıvı bir faza dönüştürmek için genellikle bir sisteme ısı uygulamak gerekir. Ekzotermik reaksiyonlara örnek olarak, bir maddenin oksijenle reaksiyona girerek enerji açığa çıkardığı basit bir yanma süreci verilebilir.
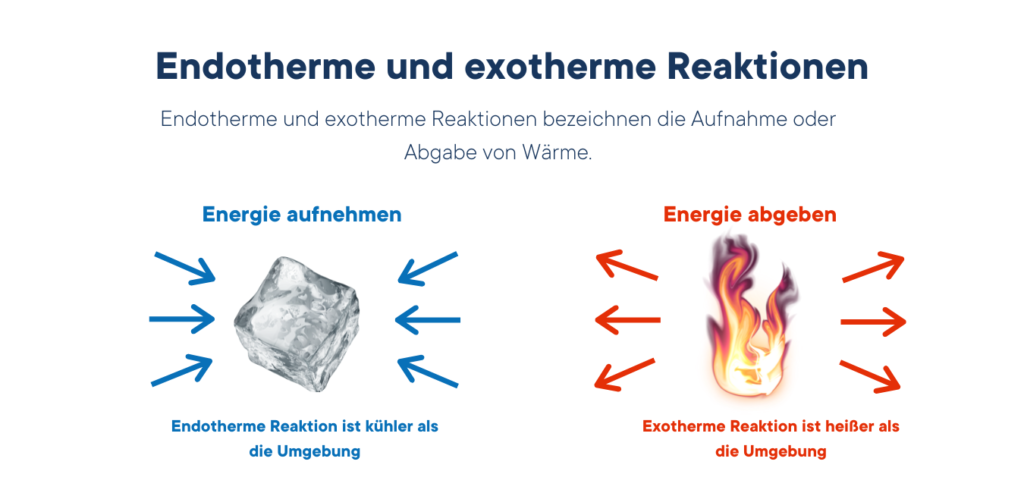
Endotermik ve ekzotermik reaksiyonlar arasındaki fark:
Endotermik:
- Enerji tüketilir (ısı emilir)
- Reaksiyon için tüketilen veya gereken enerji
- İç entalpide artış
Endotermik süreçlere örnekler şunlardır
- Tuzların çözücüler içinde çözünmesi
- Alkanların bölünmesi
- Buharlaşan sıvılar
- Eriyen katılar
Ekzotermik:
- Enerji açığa çıkar (ısı açığa çıkar)
- Reaksiyon kendiliğinden veya tetiklenmiş
- İç entalpide azalma
Ekzotermik süreçlere örnekler:
- Termit reaksiyonu
- Nötralizasyon (örneğin bir asit ve bir bazın tuz ve su oluşturmak üzere karıştırılması)
- Çoğu polimerizasyon reaksiyonları
- Yanma
- Solunum
- Metallerin korozyonu (bir oksidasyon reaksiyonu)
- Çoğu kristalleşme süreçleri
