Spis treści
Jaka jest różnica między reakcjami endotermicznymi i egzotermicznymi?
Główna różnica między reakcjami egzotermicznymi i endotermicznymi polega na wymianie ciepła z otoczeniem:
- Reakcje endotermiczne pochłaniają energię w postaci ciepła z otoczenia, co powoduje, że otoczenie staje się zimniejsze. Oznacza to, że produkty mają więcej energii niż reagenty, a reakcja wymaga ciepła, co prowadzi do dodatniej zmiany entalpii (ΔH).
- Reakcje egzotermiczne uwalniają energię do otoczenia w postaci ciepła, co powoduje, że otoczenie staje się cieplejsze. W tym przypadku produkty mają mniej energii niż reagenty, a reakcja uwalnia ciepło, co prowadzi do ujemnej zmiany entalpii (ΔH).
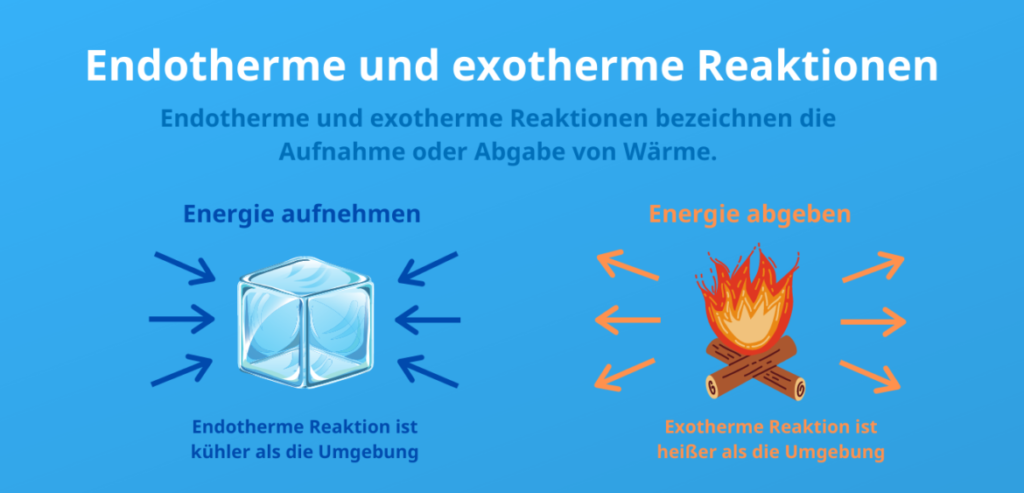
Jak rozpoznać reakcję egzotermiczną lub endotermiczną?
Istnieją dwie metody rozpoznawania reakcji egzotermicznych:
- Zmiana temperatury;
- W reakcji egzotermicznej energia jest uwalniana, co powoduje wzrost temperatury mieszaniny reakcyjnej. Z kolei w reakcji endotermicznej energia jest pochłaniana, co prowadzi do spadku temperatury. Zmiany temperatury można zaobserwować umieszczając termometr w mieszaninie reakcyjnej
- Zmiana entalpii:
- entalpia zmiana entalpii (ΔH) to różnica między energią produktów a energią reagentów. Jeśli ΔH jest ujemna, jest to egzotermiczna reakcja chemiczna, ponieważ więcej energii jest uwalniane, gdy powstają produkty, niż energia zużyta do rozbicia reagentów. Jeśli ΔH jest dodatnie, jest to endotermiczna reakcja chemiczna, ponieważ podczas tworzenia produktów uwalniana jest mniejsza ilość energii niż energia zużyta do rozkładu reagentów.
Reakcje egzotermiczne i endotermiczne mają różny wpływ na środowisko:
Reakcje egzotermiczne uwalniają ciepło do środowiska, co może mieć zarówno pozytywne, jak i negatywne skutki dla środowiska. Na przykład, są one zaangażowane w procesy takie jak oddychanie, spalanie i produkcja energii. Jednak reakcje egzotermiczne mogą również przyczyniać się do problemów środowiskowych, takich jak zanieczyszczenie powietrza i wody.
Inne przykłady reakcji egzotermicznych:
- Spalanie drewna lub węgla:
- Podczas spalania drewna lub węgla uwalniane jest ciepło, które jest egzotermiczne. Reakcje te są wykorzystywane w systemach grzewczych, piecach i silnikach do generowania energii.
- Utlenianie metali:
- Gdy metale reagują z tlenem, takie jak żelazo, tworząc rdzę, jest to reakcja egzotermiczna, w której uwalniane jest ciepło.
- Chemiczne materiały wybuchowe:
- Eksplozje w chemicznych materiałach wybuchowych są reakcjami egzotermicznymi, w których uwalniane są duże ilości energii w postaci ciepła i ciśnienia.
Reakcje endotermiczne pochłaniają ciepło z otoczenia. Chociaż są one niezbędne w procesach takich jak fotosynteza i gotowanie, generalnie mają mniejszy bezpośredni wpływ na środowisko w porównaniu z reakcjami egzotermicznymi.
Dalsze przykłady reakcji endotermicznych:
- Fotosynteza:
- W procesie fotosyntezy rośliny pochłaniają dwutlenek węgla z powietrza i przekształcają go w cukier i tlen przy użyciu energii świetlnej. Jest to reakcja endotermiczna, ponieważ energia jest pochłaniana w postaci światła
- Wrząca woda:
- Podgrzewanie wody w celu doprowadzenia jej do wrzenia jest reakcją endotermiczną. Podczas procesu wrzenia dodawana jest energia w postaci ciepła w celu przekształcenia cząsteczek wody w parę.
- Roztwór soli w wodzie:
- Kiedy sól rozpuszcza się w wodzie, cząsteczki soli absorbują ciepło z otoczenia, aby rozbić kryształy i rozproszyć się w postaci rozpuszczonej.