Spis treści
Etapy charakterystyki materiału
Gęstość, twardość, pojemność cieplna lub przewodność
Stan zagregowany
Faza jest generalnie jednorodną kompozycją w materiale. Termin faza może odnosić się do
Określanie przejść fazowych
Aby dowiedzieć się, w której fazie znajduje się materiał, a tym samym kiedy mają zastosowanie jego parametry, szczególnie ważne jest poznanie i określenie przejść fazowych materiału. Zwykle występują one po osiągnięciu określonej temperatury lub poziomu energii lub pod wpływem ciśnienia lub reakcji chemicznych.
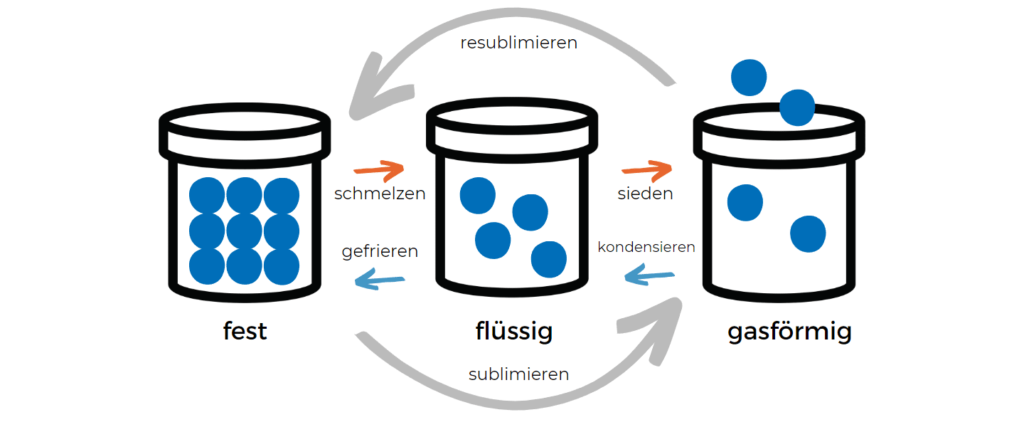
Jakie są przejścia fazowe?
Ponieważ istnieją różne definicje faz (stan skupienia, struktura krystaliczna, modyfikacja itp.), istnieją również różne przejścia fazowe. W najprostszym przypadku przejście fazowe opisuje czystą zmianę stanu skupienia, np. ze stałego w ciekły.
Przejścia fazowe są zwykle klasyfikowane zgodnie z tak zwaną klasyfikacją Ehrenfesta według Paula Ehrenfesta.
Zmienne termodynamiczne objętość, entalpia lub entropia są zwykle traktowane jako funkcja temperatury.
Przejścia fazowe są następnie podzielone na tak zwane rzędy, przy czym n-ty rząd funkcji rozważanej zmiennej ma nieciągłość w n-tej pochodnej względem temperatury. Sama funkcja i n-1 pochodna są ciągłe. W praktyce rozróżnia się tylko przejścia fazowe 1. i 2. rzędu.
Przykładami przejść fazowych 1. rzędu są
- Konwersje między stałymi, ciekłymi i gazowymi stanami skupienia, w szczególności
- Topnienie (przejście ze stanu stałego do ciekłego)
- Odparowanie (przejście z cieczy do gazu)
- Sublimacja (przejście ze stanu stałego w gazowy)
- Krzepnięcie lub zamarzanie (przejście od stanu ciekłego do stałego)
- Kondensacja (przejście od stanu gazowego do ciekłego)
- Resublimacja (przejście od stanu gazowego do stałego)
Przykładami przejść fazowych 2. rzędu są
- Zmiana między zachowaniem ferromagnetycznym i paramagnetycznym w temperaturze krytycznej lub temperaturze Curie
- Zmiana pomiędzy różnymi porządkami magnetycznymi, np. od współmiernej do niewspółmiernej struktury magnetycznej.
- Zmiana między zachowaniem ferroelektrycznym i dielektrycznym
- Przejście do nadprzewodnictwa
Jak mogę zmierzyć przejścia fazowe?
Przejścia fazowe są zwykle analizowane w analizie termicznej przy użyciu różnicowego kalorymetru skaningowego DDK (różnicowy kalorymetr skaningowy – DSC).
Jeśli substancja wykazuje przejście fazowe w mierzonym zakresie temperatur podczas pomiaru za pomocą DSC, na przykład z powodu zmiany stanu skupienia lub struktury krystalicznej, można to łatwo śledzić za pomocą DSC. Większości przejść fazowych towarzyszy pochłanianie (endotermiczne) lub uwalnianie (egzotermiczne) energii, co można wykryć jako zmianę przepływu ciepła.
DSC mierzy te zmiany temperatury za pomocą jednej lub więcej termopar, które stykają się z uchwytem próbki i w ten sposób porównują dokładną temperaturę próbki z temperaturą otoczenia i próbką referencyjną. Dokładny przepływ ciepła przez próbkę w danym czasie można następnie odczytać z różnicy między próbką referencyjną a próbką. W przypadku różnicy w przepływie ciepła między próbką a odniesieniem, znak różnicy wskazuje, czy występuje proces endotermiczny czy egzotermiczny.
Pozycja efektu, który występuje, gdy jest on wykreślany względem temperatury, również bardzo precyzyjnie wskazuje, kiedy ma on miejsce. Im dokładniej mierzona jest dokładna temperatura próbki, tym lepsza jest rozdzielczość i czułość DSC.
W przypadku przejść fazowych, zwłaszcza przejść fazowych drugiego rzędu, szybkość ogrzewania jest bardzo ważna dla tego, jak dobrze można wykryć przejście. Jeśli szybkość ogrzewania jest zbyt niska, efekty są często ledwo wykrywalne, ponieważ różnica energii między próbką a odniesieniem jest kompensowana przez piec lub grzejnik. Jeśli tempo ogrzewania jest zbyt szybkie, efekt staje się bardziej widoczny, ale jest również przesunięty do wyższych temperatur.