İçindekiler tablosu
Giriş: Protein stabilitesinin önemi
Protein stabilitesini anlamak modern biyokimya, farmasötik araştırma ve biyoteknoloji için temeldir. Protein stabilitesi sadece terapötik bir proteinin çözeltide ne kadar süre aktif kalabileceğini değil, aynı zamanda formülasyon, depolama ve taşıma için uygunluğunu da belirler (Wang 1999). Enzim mühendisliğinden ilaç geliştirme ve yapısal biyoloji çalışmalarına kadar, protein stabilitesini doğru bir şekilde değerlendirme ve optimize etme yeteneği, araştırmacıların ve yenilikçilerin yaşam bilimi uygulamalarını ilerletmelerini sağlarken, agregasyon, denatürasyon veya aktivite kaybından kaynaklanan riskleri en aza indirir.
Son yayınlar, tampon bileşimi veya sıcaklıktaki küçük değişikliklerin bile protein katlanmasını ve terapötik sonuçları önemli ölçüde etkileyebildiği ilaç formülasyonu ve biyoproseslemede protein stabilitesinin rolünü vurgulamaktadır (Durowoju ve ark. 2017).
Protein stabilitesini etkileyen faktörler
Proteinlerin işlevi büyük ölçüde üç boyutlu yapılarının bütünlüğüne, yani doğal konformasyonlarına bağlıdır. Bu yapı çeşitli fizikokimyasal faktörler tarafından bozulabilir:
- Sıcaklık: Yüksek sıcaklıklar proteinlerin çözülmesine yol açarak geri dönüşü olmayan bir işlev kaybına veya agregasyona neden olabilir.
- pH değeri: pH değerindeki değişiklikler iyonik etkileşimleri ve hidrojen bağlarını bozar, bu da yapısal kararlılığı etkiler.
- İyonik güç: Tuzlar, yüklü yan zincirlerle olan spesifik etkileşimlere bağlı olarak proteinleri stabilize veya destabilize edebilir.
- Ligand bağlanması: Proteinlere bağlanan küçük moleküller, kofaktörler veya ilaçlar belirli konformasyonları stabilize veya destabilize edebilir (Durowoju ve ark. 2017).
- Genetik mutasyonlar: Tek nokta mutasyonları stabiliteyi artırabilir veya azaltabilir ve böylece fizyolojik koşullar altında proteinin davranışını etkileyebilir.
Sistematik çalışmalar, tampon kimyasının ayarlanması ve taşıma ve depolama sırasında sıcaklığın kontrol edilmesinin protein aktivitesinin korunması için en etkili önlemler arasında olduğunu göstermektedir (Wang 1999).
Temel Bilgiler: Protein stabilitesi ne anlama gelir?
Protein stabilitesi, farklı koşullar altında bir proteinin doğal yapısının direncini ifade eder. Aşağıdakileri içerir:
- Termodinamik kararlılık: Bir proteinin katlanmış halde kalma ve denatüre olmama eğilimi.
- Kinetik kararlılık: Bir proteinin katlanmamış veya toplanmış bir duruma geçme hızı.
- Tersine çevrilebilir değişiklikler: Bazı katlanma geçişleri uygun koşulların yeniden sağlanmasıyla tersine çevrilebilir (örneğin hafif denatürasyondan sonra yeniden katlanma).
- Geri döndürülemez değişiklikler: Ağır işlemler (örn. yüksek sıcaklıklar veya kimyasal maddeler) geri döndürülemeyen kümelenmelere veya açılmalara yol açabilir.
Stabilite genellikle protein popülasyonunun yarısının denatüre olduğu erime sıcaklığı (Tm) ile ölçülür – stabilite analizlerinde ölçülen önemli bir parametredir (Durowoju ve ark. 2017).
Protein stabilitesinin değerlendirilmesi için yöntemler
Biyomoleküler stabilite ve etkileşimleri incelemek için çeşitli ortogonal teknikler geliştirilmiştir. Uygun yöntemin seçimi araştırma sorusuna, protein türüne ve mevcut ekipmana bağlıdır.
Diferansiyel taramalı kalorimetri (DSC)
DSC proteinlerin hassas stabilite çalışmaları için vazgeçilmez bir araçtır (Durowoju ve ark. 2017). Sıcaklık arttıkça bir protein örneğini açmak için gereken ısıyı ölçerek, DSC:
- Denatürasyon sıcaklığı (Tm): Termal kararlılığı gösterir.
- Entalpi değişiklikleri(ΔH): Katlanma enerji geçişlerini gösterir.
- Açılma profilleri: Tersinir veya tersinmez geçişleri karakterize edin.
DSC düşük konsantrasyonlardaki proteinler için bile ince geçişleri tespit etmedeki doğruluğu nedeniyle değerlidir ve varyantları, termal formülasyon davranışını ve ligand kaynaklı stabilite değişimlerini karakterize etmede özellikle güçlüdür (Bir DSC Yönteminin Kalifikasyonu 2020).
Diğer analiz yöntemleri
Dinamik ışık saçılımı (DLS): Hidrodinamik yarıçapı ölçer ve protein agregasyonunu tanır, ayrıca termal kararlılık testleri (Mirasol ve ark. 2021).
UV-Vis spektroskopisi: Aromatik yan zincirler veya kromoforlarla ilişkili absorbans değişikliklerini izleyerek katlanmayı izler.
İzotermal titrasyon kalorimetrisi (ITC): Proteinler ve ligandlar arasındaki bağlanma etkileşimlerini ölçer; ligand birleşmesi üzerine stabilite değişikliklerini tespit etmek için yararlıdır (Durowoju et al. 2017).
Dairesel dikroizm (CD) spektroskopisi: Katlanma veya denatürasyon sırasında ikincil yapıdaki değişiklikleri araştırır (örn. alfa sarmaldan beta kıvrımlı tabakaya geçişler).
Kararlılığı etkileyen etkileşimlerin araştırılması
Proteinler moleküler çevreleriyle sürekli etkileşim halindedir. Bu etkileşimlerin kararlılığı nasıl etkilediğini değerlendirmek araştırma ve geliştirme için çok önemlidir:
- Ligand bağlanması: DSC ve ITC, küçük moleküllerin, ilaçların ve kofaktörlerin bağlanma afinitelerini ve stabilize edici veya destabilize edici etkilerini belirlemek için kullanılır (Durowoju et al. 2017)
- Protein agregasyonu: DLS, ısıya veya strese maruz kalma sırasında agregasyon eğilimindeki değişiklikleri tanımlar (Wang 1999).
- pH bağımlılığı: Araştırmacılar, farklı pH değerlerinde DSC çalışmaları gerçekleştirerek protonasyon durumlarının katlanmadaki rolü hakkında bilgi ediniyor.
- Genetik varyantlar: DSC ve DLS kullanılarak Tm veya agregasyon profillerinin karşılaştırılması, nokta mutasyonlarından veya tasarlanmış sekans değişikliklerinden kaynaklanan stabilitenin değerlendirilmesine olanak tanır (Mirasol ve ark. 2021).
Termal yöntemler moleküler etkileşimlere nasıl ışık tutuyor?
Termal teknikler, örneğin DSC sadece Tm ve entalpi sağlamakla kalmaz, aynı zamanda ligand veya tampon titrasyon protokolleri ile birlikte bağlanma yakınlıkları ve yapısal stabilizasyon hakkında derin bilgiler sunar (Durowoju ve ark. 2017). Örneğin, bir proteinin Tm’sini artıran bir ligand, bir ilacın tasarımı veya formülasyonu ile ilgili doğrudan stabilize edici bir etkileşimi gösterir.
Pratik bilgiler ve ölçüm parametreleri
Protein stabilite verilerinin yorumlanması, deneysel koşulların ve tipik sonuçların dikkate alınmasını gerektirir:
- Isıtma hızı: Kinetik ve termodinamik kararlılığın tespitini etkiler; daha yavaş hızlar denge ölçümlerini destekler.
- Numune konsantrasyonu: Yeterli bir konsantrasyon, agregasyon paraziti olmadan güvenilir bir sinyal sağlar.
- Tampon bileşimi: Farklı tamponların ve eksipiyanların Tm ve dekonvolüsyon entalpisi üzerindeki stabilize edici etkilerini karşılaştırın (Wang 1999).
- Kontrol numuneleri: Her zaman iyi tanımlanmış standartlarla karşılaştırın, örneğin vahşi tip ve mutant proteinler veya sadece tampon kontrolleri.
Uygulama
Uygulama örnekleri
- Formülasyon geliştirme için monoklonal antikorların stabilite profillerinin karşılaştırılması (bir DSC yöntem 2020).
- Termal stabilite gerektiren endüstriyel biyokataliz için enzim varyantlarının değerlendirilmesi.
- İlaç keşfi ve yapısal biyolojinin erken evresinde protein-ligand bağlanma afinitelerinin taranması (Durowoju ve ark. 2017).
Uygulama örneği: Lizozimin termal denatürasyonu
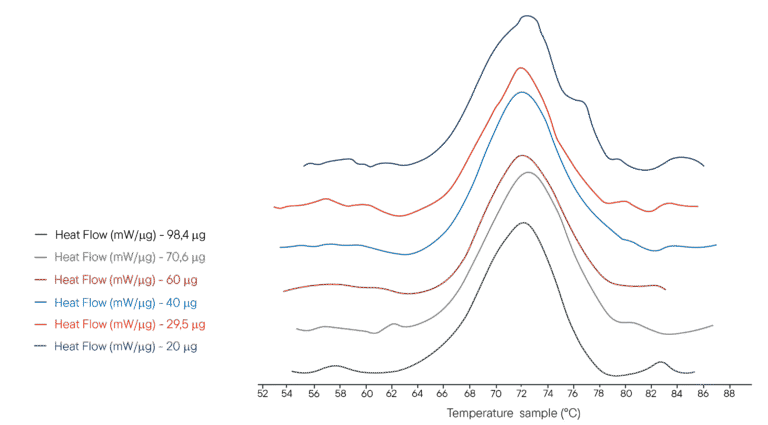
PHB tamponundaki farklı lizozim çözeltilerinden 100µl, 100µl’lik bir krozeye eklenmiştir. Her biri analiz edilen lizozimin farklı kütlelerini temsil eden farklı konsantrasyonlar kullanılmıştır. Referans kroze aynı hacimde PHB tamponu ile doldurulmuştur. Ultimate DSC, 1°C/dk’da 40°C’den 95°C’ye bir sıcaklık artışı gerçekleştirecek şekilde programlanmıştır.
Ultimate DSC ile lizozimin entalpi ve denatürasyon sıcaklığı, mevcut cihazlara kıyasla 5 ila 10 daha az numune ile ölçülebilir. Her bir termogram 60 dakikadan daha kısa bir sürede oluşturularak hızlı analiz yapılmasını sağlar. Ultimate DSC büyük miktarda numuneden tasarruf sağlar ve daha hızlı çalışmanıza olanak tanır.
Araştırmanız için doğru yöntemi seçin
En uygun analitik yöntemin seçimi, spesifik proteininize, araştırma hedefinize ve mevcut kaynaklarınıza bağlıdır:
| Method | Key Insights | Typical Applications |
|---|---|---|
| DSC | Tm, ΔH, unfolding profile | Formulation, variant screening, stability assays |
| DLS | Aggregation, size distribution | Formulation, quality control, aggregation analysis |
| ITC | Binding affinity, thermodynamics | Drug design, ligand screening, protein-protein interactions |
| CD-Spectroscopy | Secondary structure change | Conformational studies, denaturation monitoring |
| UV/Vis Spectroscopy | Folding/unfolding, aggregation | Quick screening, routine assay |
Ayrıntılı bir karşılaştırma için, son incelemeler, hassas kalorimetrik ve spektroskopik ölçümler de dahil olmak üzere birden fazla tekniğin entegrasyonunun, protein stabilitesinin ve sonraki uygulamalar için uygunluğunun sağlam bir değerlendirmesine nasıl yol açtığını vurgulamaktadır (Mirasol ve ark. 2021; Durowoju ve ark. 2017).
Sonuç ve sonraki adımlar
Protein stabilitesini anlamak ve kontrol etmek, başarılı biyomolekül araştırması, farmasötik formülasyon ve ilaç geliştirmenin merkezinde yer alır. Termal analiz, özellikle de DSC, gerçek dünya koşulları altında protein davranışına ilişkin sağlam, ölçülebilir bilgiler sağlayarak veriye dayalı kararları güvenle almanıza yardımcı olur.
Protein stabilitesi çalışmalarınızı ilerletmek istiyorsanız, Linseis UDSC L64 son teknoloji ürünü kalori̇metri̇ Biyomoleküler analiz ve formülasyon geliştirme için özel olarak tasarlanmış yetenekler. Kalorimetri Çözümleri sayfamızda UDSC L64’ün performansı ve çok yönlü uygulama yelpazesi hakkında daha fazla bilgi edinin veya araştırma gereksinimlerinizle ilgili bireysel tavsiye almak için uzman ekibimizle iletişime geçin.
İleri okuma için seçilmiş literatür
- Durowoju, I.B., Bhandal, K.S., Hu, J., Carpick, B. ve Kirkitadze, M. (2017) Differential Scanning Calorimetry-A Method for Assessing the Thermal Stability of Proteins, Journal of Visualised Experiments, (121), e55262. https://pmc.ncbi.nlm.nih.gov/articles/PMC5409303/
- Wang, W. (1999) ‘Sıvı protein ilaçlarının kararsızlığı, stabilizasyonu ve formülasyonu’, International Journal of Pharmaceutics, 185(2), s. 129-188. https://doi.org/10.1016/S0378-5173(99)00152-0
- Mirasol, F., Wypych, J. ve Kopec, B. (2021) Stability Testing of Protein Therapeutics Using DLS, Pharmaceutical Technology. https://www.pharmtech.com/view/stability-testing-of-protein-therapeutics-using-dls
- Monoklonal antikorların biyofiziksel karakterizasyonu için diferansiyel taramalı kalorimetri yönteminin kalifikasyonu (Açık Erişim). https://www.openaccessjournals.com/articles/qualification-of-a-differential-scanning-calorimetry-method-for-biophysical-characterization-of-monoclonal-antibodies-an.pdf