本研究では、硝酸カルシウム四水和物-Ca(NO3)2.
4H2O– のTG-DSC測定結果を示し、考察する。
この塩は、安価で非常に効果的であるため、蓄熱および熱伝達の材料として既に広く使用されている。
サンプルは、重量変化とDSCシグナルを同時にモニターするLinseis STA PT 1000装置を用いて分析した。
DSCシグナルからエンタルピーの 相転移のエンタルピーと 熱容量を求めることができる。
試料を密閉アルミるつぼの中で、10 K/分の加熱速度で180 °Cまで加熱し、3時間等温に保った。その後、10K/分の加熱速度で600℃まで加熱した。
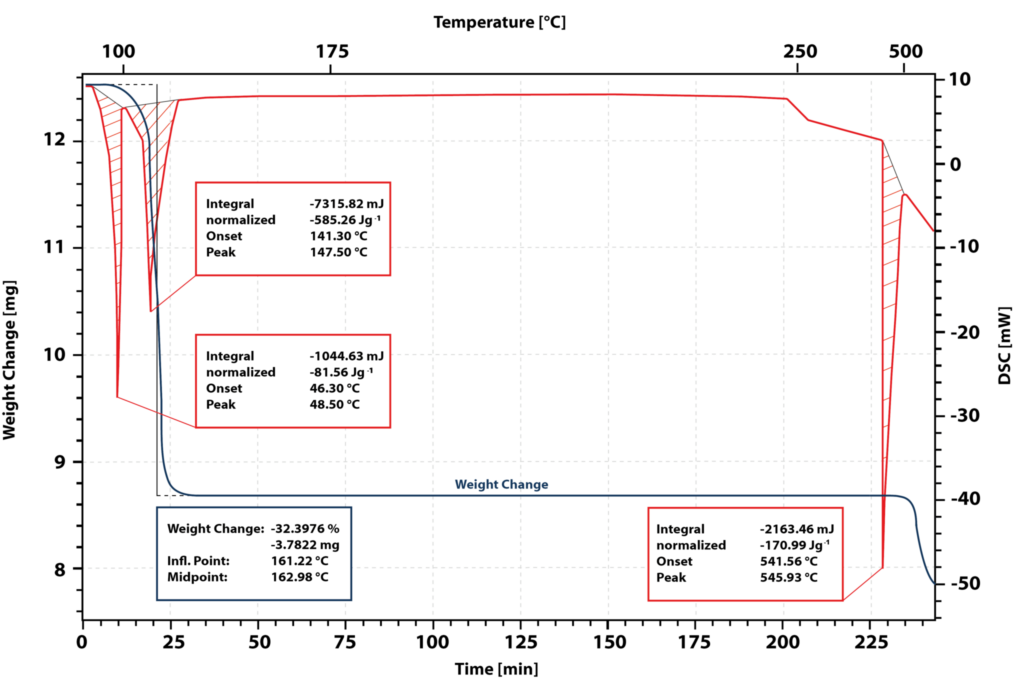
青い曲線は質量損失を、赤い曲線はDSCシグナルを示す。
DSC信号の最初のピークは試料の融解によるものである。
融解ピークの開始点は46℃である。
試料が完全に融解した後、141 °Cでオンセットする第二の吸熱ピークが発生する。
TGシグナルは、この温度範囲で32%の重量減少を示している。
硝酸カルシウム四水和物の結晶水が分離し、固体の無水塩が形成される。
180℃での等温保持時間中、試料はそれ以上変化しない。つまり、この温度は塩を乾燥させ、無水塩を得るのに理想的である。
再び541℃まで加熱すると吸熱ピークが生じる。
無水塩は融解する。
しかし、TGシグナルは重量の減少を示す。
これは塩が融解中に分解することを示している。
したがって、溶融した無水塩の融解エンタルピーと熱容量を直接測定することはできません。
しかし、これは塩混合物のTG-DSC測定をさらに進めることで達成できる。
硝酸カルシウムは、硝酸リチウム、硝酸ナトリウム、硝酸カリウムと異なるモル比率で混合しなければならない。
融解のエンタルピーは、混合物のDSC融解ピークから求めることができる。
そして、純粋な硝酸カルシウムの融解エンタルピーは、硝酸カルシウムに対するモル割合が100%になるように外挿することで、単純に計算することができる。
同じ方法で溶融無水硝酸カルシウムの熱容量も測定できる。
