目次
吸熱反応と発熱反応の違いとは?
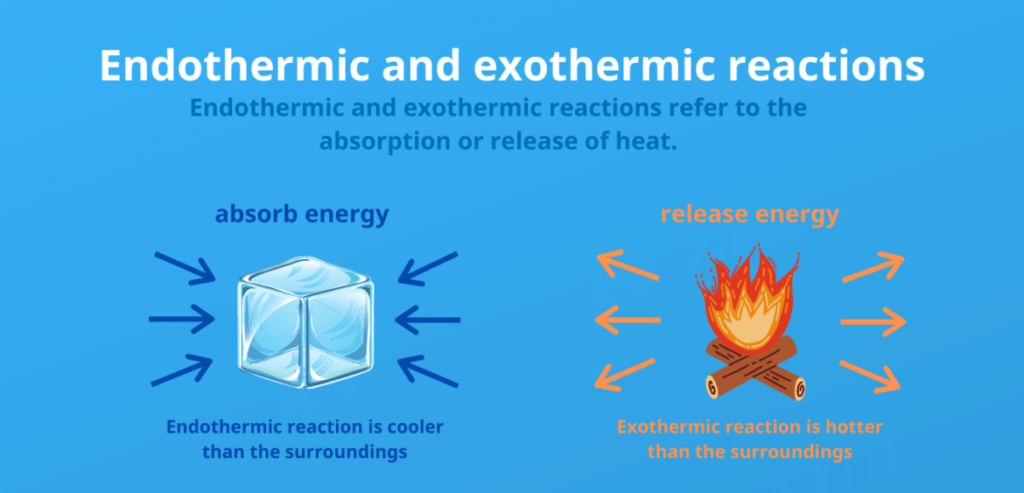
発熱反応と吸熱反応の主な違いは、周囲との熱交換にある:
- 吸熱反応は、周囲から熱の形でエネルギーを吸収する。は周囲から熱の形でエネルギーを吸収し、周囲が冷たくなる。 これは、生成物が反応物より多くのエネルギーを持つことを意味し、反応は熱を必要とし、エンタルピー(ΔH)の正の変化につながる。
- 発熱反応はエネルギーをを熱の形で周囲に放出し、周囲が暖かくなる。 この場合、生成物は反応物よりエネルギーが少なく、反応は熱を放出し、エンタルピー(ΔH)の負の変化をもたらす。
発熱反応と吸熱反応の見分け方は?
発熱反応を認識するには2つの方法がある:
- 温度変化:
- 発熱 反応ではエネルギーが放出され、反応混合物の温度が上昇する。 一方、吸熱 反応ではエネルギーが吸収され、温度が低下する。 温度計を反応混合物の中に入れて、温度の変化を観察することができる。
- エンタルピーの変化:
- エンタルピーの変化(ΔH)は、生成物のエネルギーと反応物のエネルギーの差である。 ΔHが 負の場合 、反応物を分解するために使われるよりも、生成物が形成されるときに放出されるエネルギーの方が大きいので、発熱性 化学 反応を 示す。 Δ Hが 正の場合 、反応物を分解するのに使われるエネルギーよりも、生成物が生成されるときに放出されるエネルギーの方が少ないため、吸熱 化学 反応 であることを 示す。
発熱反応と吸熱反応は環境に異なる影響を与える:
発熱反応は環境に熱を放出し、環境にプラスとマイナスの両方の影響を与える可能性がある。 発熱反応は、呼吸、燃焼、エネルギー生産などのプロセスに関与している。 しかし、発熱反応は大気汚染や水質汚濁などの環境問題を引き起こすこともある。
発熱反応のさらなる例:
- 薪や石炭の燃焼:
- 木材や石炭の燃焼は熱を放出し、発熱反応となる。 このような反応は、ヒーター、炉、エンジンなどのエネルギー生産に利用される。
- 金属の酸化:
- 鉄が錆を作るように、金属が酸素と反応するとき、それは熱が放出される発熱反応である。
- 化学爆薬:
- 化学火薬の爆発は発熱反応であり、熱と圧力の形で大量のエネルギーを放出する。
吸熱反応は周囲から熱を吸収する。 光合成や調理のようなプロセスには欠かせないが、一般的に発熱反応に比べ環境への直接的な影響は少ない。
吸熱反応のさらなる例:
- 光合成:
- 光合成では、植物は空気中の二酸化炭素を吸収し、光エネルギーを使って糖と酸素に変換する。 これは、光というエネルギーが吸収されるため、吸熱反応である。
- 沸騰水:
- 水を加熱して沸騰させるのは吸熱反応である。 沸騰の過程で、熱というエネルギーが供給され、水の粒子が蒸気に変わる。
- 塩を水に溶かす:
- 塩を水に溶かすと、塩の分子は周囲から熱を吸収して結晶を壊し、溶けた状態で分散する。