الصيغة الكيميائية للجبس هي CaSO4 ∙ 2H2O(ثنائي هيدرات كبريتات الكالسيوم). هناك مجموعة متنوعة من الاستخدامات للجبس كمادة بناء.
الجص عبارة عن مسحوق جاف يتم خلطه بالماء لتشكيل عجينة تتصلب بعد ذلك. ويبقى طرياً إلى حد ما بعد التجفيف ويمكن عمله بسهولة باستخدام أدوات معدنية.
يتفاعل ثنائي هيدرات كبريتات الكالسيوم (CaSO4 ∙ ½H2O) مع الماء لتكوين ثنائي هيدرات كبريتات الكالسيوم ويعود ثنائي هيدرات كبريتات الكالسيوم لفصل الماء عند تسخينه واستبداله بهيميهيدرات كبريتات الكالسيوم.
وتنتج قابلية انقسام بلورة CaSO4 ∙ 2H2Oعن طبقات ثنائية CaSO4(في كل طبقة من أيونات Ca2 + وSO4 2 بالتناوب بجانب بعضها البعض) مع روابط هيدروجينية منخفضة نسبيًا.
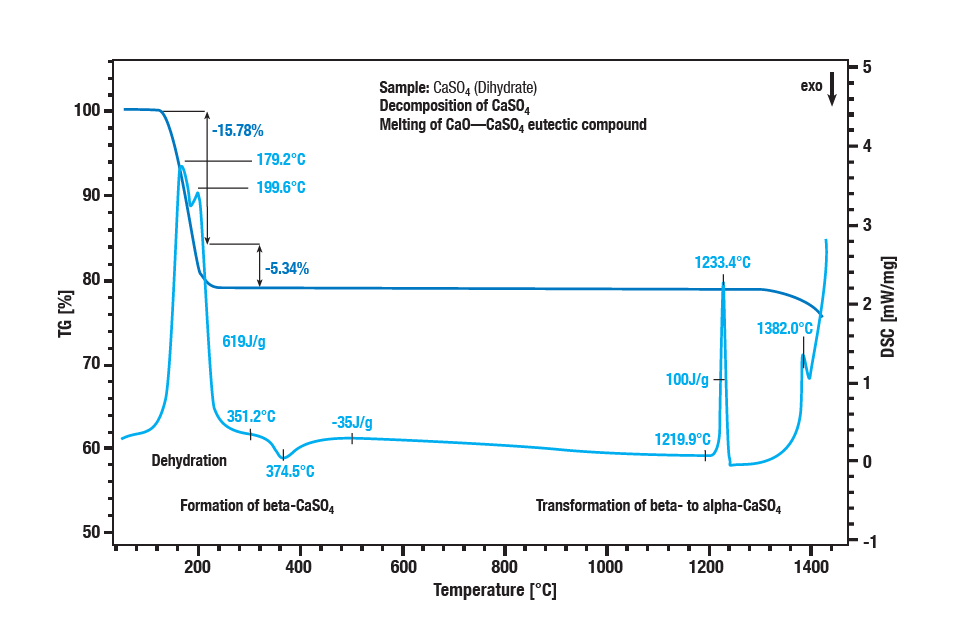
تحدث عملية تجفيف ثنائي هيدرات كبريتات الكالسيوم على مرحلتين بين 100 درجة مئوية و300 درجة مئوية. وتتمثل الخطوة الأولى في تكوين ثنائي هيدرات الهيميهيدرات (CaSO4 ∙ 2H2Oإلى CaSO4 ∙ ½H2O).
ويشكل المزيد من الجفاف الأنهيدرات (CaSO4 ½ H2Oإلى CaSO 4). وبتأثير طارد للحرارة عند درجة حرارة 340 درجة مئوية تقريبًا، يتحول الأنهيدرات إلى كبريتات الكالسيوم بيتا. التأثير الطارد للحرارة في المنحنى عند درجة حرارة 1220 درجة مئوية تقريبًا هو تحول كبريتات بيتا-كالسيوم-كولفونات بيتا إلى كبريتات ألفا-كالسيوم. ينعكس تحلل الكبريتات في فقدان إضافي للكتلة عند درجات حرارة أعلى من 1250 درجة مئوية.
تتحول كبريتات الكالسيوم إلى أكسيد الكالسيوم. يبلغ ذوبان خليط سهل الانصهار من كبريتات الكالسيوم وأكسيد الكالسيوم ذروته عند 1380 درجة مئوية.

